

Antonio F. Radicioni, Antonella Anzuini, Francesco Carlomagno
UOD Diagnostica ormonale, Seminologia e Banca del seme – Policlinico Umberto I
Dipartimento di Medicina Sperimentale, Sezione di Fisiopatologia Medica. Sapienza Università di Roma
L’ormone anti-Mülleriano (AMH) è una glicoproteina appartenente alla superfamiglia del TGF-β, inizialmente identificato come responsabile della differenziazione dell’apparato genitale maschile.
L’AMH è prodotto come pro-ormone costituito da due monomeri, uniti mediante ponti disolfuro, che subiscono un clivaggio proteolitico a formare due omodimeri: il primo costituito dalle pro-regioni Nterminali e l’altro dalle regioni mature C-terminali. Questi rimangono legati in maniera non-covalente a formare un complesso circolante di 140 kDa.
Attualmente sono disponibili sistemi di dosaggio per la determinazione della concentrazione di AMH che, utilizzando metodiche ELISA a sandwich e anticorpi monoclonali diretti sia contro epitopi della regione matura che della pro-regione, raggiungono elevata sensibilità (fino a 0,08 ng/mL con kit di seconda generazione). Tali sistemi sono tuttavia gravati da importanti limitazioni: l’assenza di uno standard internazionale di riferimento per la calibrazione e la mancata comparabilità con i risultati dei precedenti kit, cui si aggiungono dubbi riguardo alla stabilità dell’AMH durante la conservazione e la lavorazione del campione.
Nel maschio l’AMH è secreto dalle cellule di Sertoli (CS) immature e, durante la vita fetale, è responsabile della regressione dei dotti di Müller verso l’ottava-nona settimana di gestazione. I livelli di AMH sono relativamente ridotti alla nascita, ma tendono ad aumentare nei primi 6-9 mesi di vita (minipubertà), riflettendo una proliferazione delle CS conseguente all’incremento dei livelli dell’FSH. Le concentrazioni dell’ormone si mantengono relativamente stabili ed elevate durante l’infanzia e la tarda pre-pubertà. All’inizio dello sviluppo puberale, l’incremento del testosterone determina un’ulteriore maturazione/differenziazione delle CS e down-regolazione dell’espressione del gene dell’AMH cui consegue un rapido e progressivo decremento dei valori dell’ormone sertoliano. Da questa fase, l’AMH viene rilasciato principalmente nel lume dei tubuli seminiferi, con livelli nel plasma seminale maggiori rispetto a quelli sierici.
In casi di gonade bilateralmente non palpabile il dosaggio dell’AMH può essere impiegato nella diagnostica differenziale tra il criptorchidismo bilaterale e l’anorchia o la disgenesia gonadica. Inoltre, durante l’infanzia, l’ormone costituisce l’unico marker di funzione sertoliana utilizzabile, insieme all’inibina-B; al contrario, dopo la pubertà e nell’uomo adulto il notevole decremento dei valori di AMH non ne consentono un impiego diagnostico (Tabella 2).
Nella donna l’AMH è espresso dalle cellule della granulosa (CG) dei piccoli follicoli in sviluppo, dalla fase di reclutamento dei follicoli primordiali fino allo stadio di follicoli pre-antrali e piccoli follicoli antrali (fino a 8 mm di diametro). Esso funge da fattore di sopravvivenza per i piccoli follicoli in sviluppo riducendone la sensibilità all’FSH e la crescita dei follicoli pre-antrali indotta dallo stesso. Agisce inoltre da regolatore della produzione estrogenica follicolare: assicura così che ciascun piccolo follicolo antrale produca bassi livelli di estradiolo prima della selezione.
Nella donna si osserva un picco nei livelli sierici di AMH poco dopo la nascita che, nel tempo, aumenta progressivamente fino a raggiungere un picco intorno ai 25 anni di età, seguito da un costante declino fino a livelli non più rilevabili all’inizio della menopausa.
Sebbene i livelli di AMH mostrino un’elevata variabilità inter-individuale nella donna, la variabilità intraindividuale è funzione principalmente dell’età, con fluttuazioni minime durante il ciclo mestruale. Una riduzione significativa si osserva tuttavia in seguito a soppressione ovarica mediante interventi farmacologici o durante la gravidanza.
I valori di AMH (Tabella 2) sono utilizzati per predire la risposta ovarica e personalizzare la terapia durante le procedure di fecondazione in vitro, nella valutazione del danno della riserva follicolare ovarica indotto da fonti iatrogene, quali radio- o chemioterapia, per predire l’età di insorgenza della menopausa, quale possibile criterio diagnostico nella sindrome dell’ovaio policistico (PCOS) ed eziologico nell’insufficienza ovarica prematura (POF).
Tabella 1 - Valori di riferimento dell’AMH sierico in diversi gruppi di soggetti normali
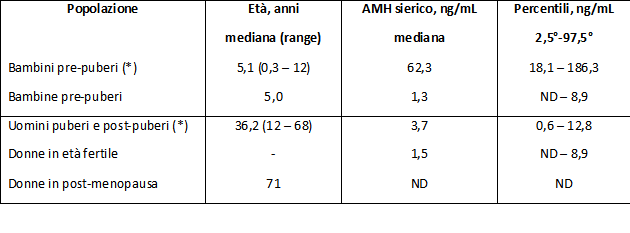
Metodica di riferimento: Beckman Coulter AMH Gen II ELISA. ND: non determinabile, inferiore ai limiti di rilevazione della metodica.
(*) Dati degli autori
Tabella 2 - Valore diagnostico del dosaggio di AMH
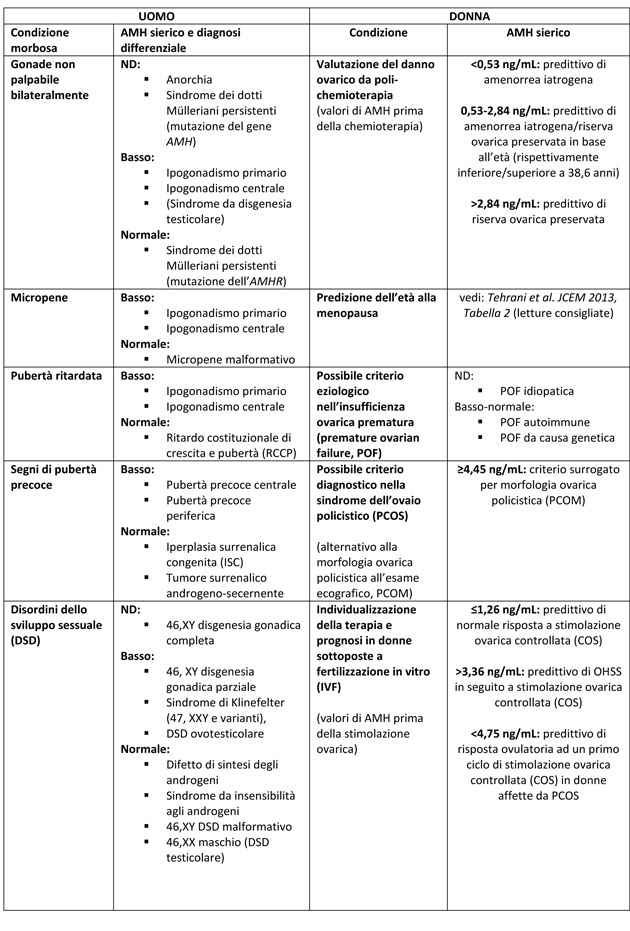
Letture consigliate: