

Alessandro Ilacqua, Giulia Izzo, Antonio Aversa
Dipartimento di Medicina Sperimentale e Clinica, Università Magna Graecia, Catanzaro. Corrispondenza:
Prof. Antonio Aversa, Dipartimento di Medicina Sperimentale e Clinica, Università Magna Graecia
Catanzaro. [email protected]
Le disfunzioni tiroidee (DT), oltre che i noti effetti sistemici, presentano effetti emergenti sulla funzione sessuale e riproduttiva maschile. Gli studi pre-clinici hanno dimostrato che gli ormoni tiroidei (OT) possono concorrere alla regolazione la funzione sessuale attraverso tre meccanismi putativi: il controllo della secrezione di testosterone da parte del cellule del Leydig, soprattutto in epoca peri-puberale; il controllo periferico sulla muscolatura liscia dei corpi cavernosi, attraverso il legame con le identificate isoforme recettoriali TRα1 e TRα2 [1]; e il controllo periferico sulla muscolatura liscia delle vescichette seminali, delle ampolle deferenziali e della muscolatura periprostatica modulando la funzione dei recettori adrenergici e l’attività simpatica. Gli studi clinici confermano che l’ipertiroidismo conclamato e sub-clinico presentano un’incidenza maggiore di disfunzione erettile (DE) rispetto all’ipotiroidismo clinico e subclinico. [2] La severità della DE correla positivamente con il grado di DT ed il ripristino dell’eutiroidismo corregge la DE e migliora diversi aspetti della sessualità (desiderio, funzione sessuale, controllo eiaculatorio).[1] Anche i disturbi eiaculatori, oltre che dai livelli plasmatici di testosterone e prolattina, sono influenzati dagli OT. L’ipertiroidismo si associa a un’aumento dell’incidenza di eiaculazione precoce (EP) a causa dell’aumento dell’attività simpatica e della contrattilità della muscolatura liscia uro-genitale. Al contrario, l’ipotiroidismo è associato ad una maggiore frequenza di eiaculazione ritardata. Le linee guida internazionali non raccomandano il dosaggio degli ormoni tiroidei nello screening della DE o della EP in quanto l’incidenza appare al di sotto di 1%, come anche in presenza di disturbi da desiderio sessuale ipoattivo [3]. (v. Tabella 1)
Gli OT, in particolare la T3, dopo deiodinazione da parte delle desiodasi testicolari, si lega al TRα1 presente negli spermatogoni e negli spermatociti e può esercitare effetti diretti anche sulla spermatogenesi [1]. Tuttavia, nella pratica clinica, le DT hanno un modesto impatto sulla fertilità maschile (v. Tabella 1), riducendo transitoriamente il numero e la motilità spermatica, e il loro trattamento può migliorare i parametri seminali. Uno studio ha dimostrato che la supplementazione con selenio può essere utile a migliorare la conta nemaspermica, la motilità e la morfologia [4]. Viceversa, la supplementazione iodica sembra avere effetti contrastanti, in quanto uomini infertili che assumono regolarmente il sale iodato presentano concentrazioni seminali ed urinarie più alte di iodio e parametri spermatici (motilità e morfologia) alterati rispetto ai controlli [5]. Il trattamento radiometabolico non sembra avere peggiorativi sui parametri seminali come non vi sono dati conclusivi sugli outcomes riproduttivi in pazienti che assumono trattamento con levo-tiroxina.
In conclusione, possiamo affermare che la condizione di eutiroidismo appare necessaria ed indispensabile affinché non si incrementi la possibilità di incorrere in disturbi della sessualità maschile; anche se per la fertilità questo dato non è chiaro, è auspicabile che anche il paziente infertile non sia affetto da una DT.
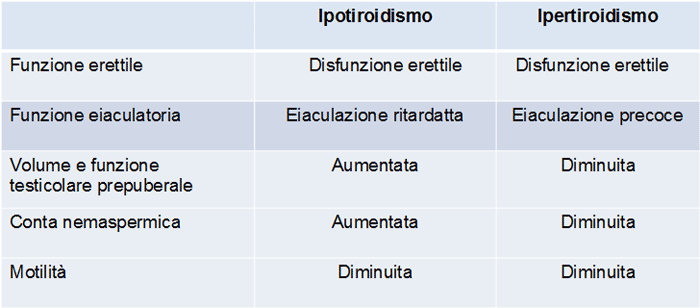
Tabella 1. Disfunzioni tiroidee e correlati con la funzione sessuale e riproduttiva maschile
Riferimenti Bibliografici