Gestione pratica del paziente affetto da malattia di Paget dell'osso
Alessia Pusterla1, F. Fraire1, L. Sauro1, M. Barale2, Massimo Procopio1
1Divisione di Endocrinologia, Diabetologia e Malattie Metaboliche, 2Divisione di Endocrinologia Oncologica, Dipartimento di Scienze Mediche, Università degli Studi di Torino, Torino, Italia
Autore corrispondente: Massimo Procopio [email protected]
Divisione di Endocrinologia, Diabetologia e Malattie Metaboliche; Dipartimento di Scienze Mediche, Università di Torino Corso AM Dogliotti 14, 10126 Torino Tel.0116709562 Cell. 3388579567 Fax 0116334769
Introduzione
La malattia di Paget dell’osso (MdP) è un disordine osteometabolico frequente nell’età avanzata (1-2% dopo i 40 anni) con una lieve predilezione per il maschio [1]. L’eziologia implica l’interazione di fattori genetici e ambientali. La mutazione del gene SQSTM1, codificante per la proteina p62, è presente nel 40-50% delle forme familiari e nel 5-10 % di quelle sporadiche [2] mentre tra i fattori ambientali le infezioni da Paramixovirus sono predominanti.
La MdP è caratterizzata da un accelerato rimodellamento osseo focale dovuto ad iperattività ed aumento di dimensioni degli osteoclasti con un’iniziale fase litica di intenso riassorbimento. Fanno seguito una fase compensatoria di neoformazione ossea da parte degli osteoblasti, che producono tessuto osseo strutturalmente disorganizzato, aumentato di volume ed ipervascolarizzato, ed una fase finale sclerotica. Le lesioni pagetiche (LP) progrediscono lentamente nell’ambito del segmento osseo colpito, sono meno compatte e più esposte alle fratture e alle deformità. La MdP può esordire in forma monostotica (10-35%) oppure poliostotica con interessamento prevalente dello scheletro assiale (pelvi e colonna lombare: 50-75%; cranio: 40%), [3].
Diagnosi
La maggior parte dei pazienti sono asintomatici mentre la presenza di sintomi o di complicanze quali dolore osseo con esacerbazione notturna, deformità e fratture scheletriche, sordità e fenomeni artrosici sono, ad oggi, molto meno frequenti. Altre possibili manifestazioni di malattia sono rappresentate da ipercalcemia, ipercalciuria, nefrolitiasi, iperuricemia, calcificazioni vascolari, alterazioni della tolleranza glucidica, ipertensione arteriosa sistolica e differenziale, scompenso cardiaco ad alta gittata e, raramente, osteosarcoma (< 1%) [2-4].
Il work-up diagnostico della MdP comprende l’esecuzione di radiogrammi mirati sulle sedi ossee colpite, la scintigrafia ossea con bisfosfonato marcato (BF) con Tc99 e la determinazione di ALP (Fig.1).
Nei pazienti con MdP asintomatica o sintomatica e riscontro Rx di lesione ossea suggestiva, l’indagine successiva è rappresentata dalla scintigrafia ossea con BF-Tc99 per la valutazione dell’estensione complessiva delle sedi colpite che saranno quindi sottoposte ad esame radiografico mirato. L’esame biochimico di screening per valutare la presenza di MdP metabolicamente attiva è la determinazione di ALP, in combinazione con i test di funzionalità epatica. In caso di forte sospetto clinico a fronte di valori di ALP di norma, è possibile valutare altri markers di formazione ossea quali la fosfatasi alcalina ossea (BAP), il propeptide N-terminale del procollagene tipo 1 (P1NP) o di riassorbimento come il beta CTx sierico o l’NTx urinario, utili soprattutto nei pazienti con disordini epatobiliari. La determinazione di BAP è indicata inoltre in caso di patologia monostotica in cui ALP risulta di norma nel 60% dei casi [2-3].
I pazienti con MdP asintomatica e riscontro di ALP elevata, in cui i radiogrammi di addome, cranio e tibie, sono in grado di evidenziare il 93% delle LP (Fig.1), saranno sottoposti successivamente alla scintigrafia ossea [2]. L’esame Rx con rilievo delle alterazioni peculiari, quali ispessimento corticale e trabecolare, incremento dimensionale e deformità delle ossa, perdita di distinzione tra corticale e midollare e presenza di aree litiche e di osteosclerosi, rappresenta il gold standard diagnostico della MdP mentre l’esame scintigrafico è più sensibile nel rilevare le LP. Anche la scintigrafia ossea può presentare falsi negativi rappresentati da LP in fase di quiescenza mentre i falsi positivi sono dovuti ad osteomielite, artriti, lesioni tumorali e displasia fibrosa [2-3]. In questi casi, la diagnostica differenziale (Fig.1) si avvale di ulteriori esami quali TC, RM, PET con FDG-F18 e, laddove indicata, di una biopsia ossea per la diagnosi definitiva. La TC e la RM sono inoltre utili per la valutazione delle complicanze quali le fratture ossee, l’invaginazione basilare, la stenosi spinale e l’osteosarcoma [2-3].
Terapia
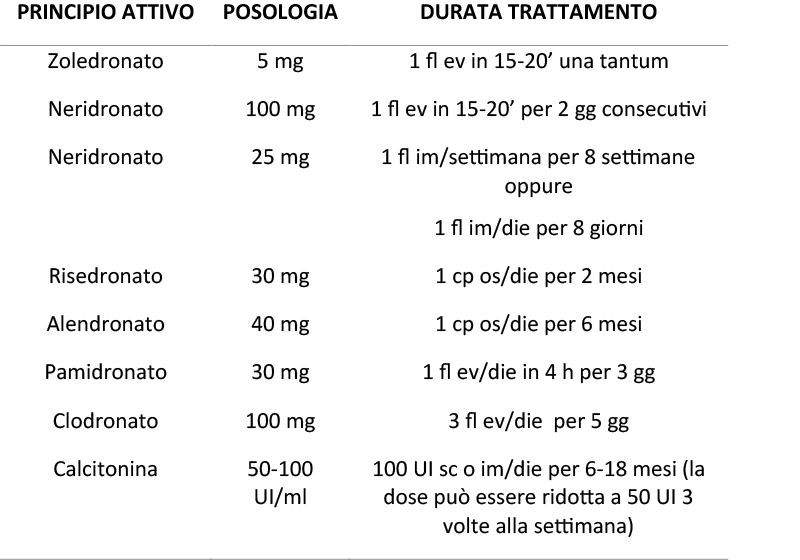
Le indicazioni alla terapia farmacologica (Tab.1), sono rappresentate dal dolore osseo oppure da LP metabolicamente attive in segmenti ossei a maggior rischio di complicanze (femore, corpi vertebrali, cranio). Il BF di prima scelta è l’acido zoledronico in singola somministrazione ev, ad azione rapida ed efficace sul dolore osseo e sulla normalizzazione di ALP [2-3]. È indispensabile la correzione dell’ipovitaminosi D e l’adozione di una dieta normo calcica prima del trattamento con BF.
Prognosi e follow-up
La MdP presenta una prognosi favorevole; infatti, la normalizzazione di ALP a 6 mesi dall’infusione di zoledronato è associata al mantenimento della remissione nel 90% dei pazienti a 6 anni [3]. Fattori predittori di recidiva di malattia sono: elevati livelli di BAP al basale e 6 mesi post-zoledronato, la presenza di malattia poliostotica e l’età meno avanzata [5].
Il monitoraggio annuale comprende la determinazione di ALP [2-3] e l’esecuzione di un esame Rxgrafico mirato sui segmenti ossei sottoposti a carico, sedi di lesioni litiche.
Fig.1 Work-up diagnostico della Malattia ossea di Paget
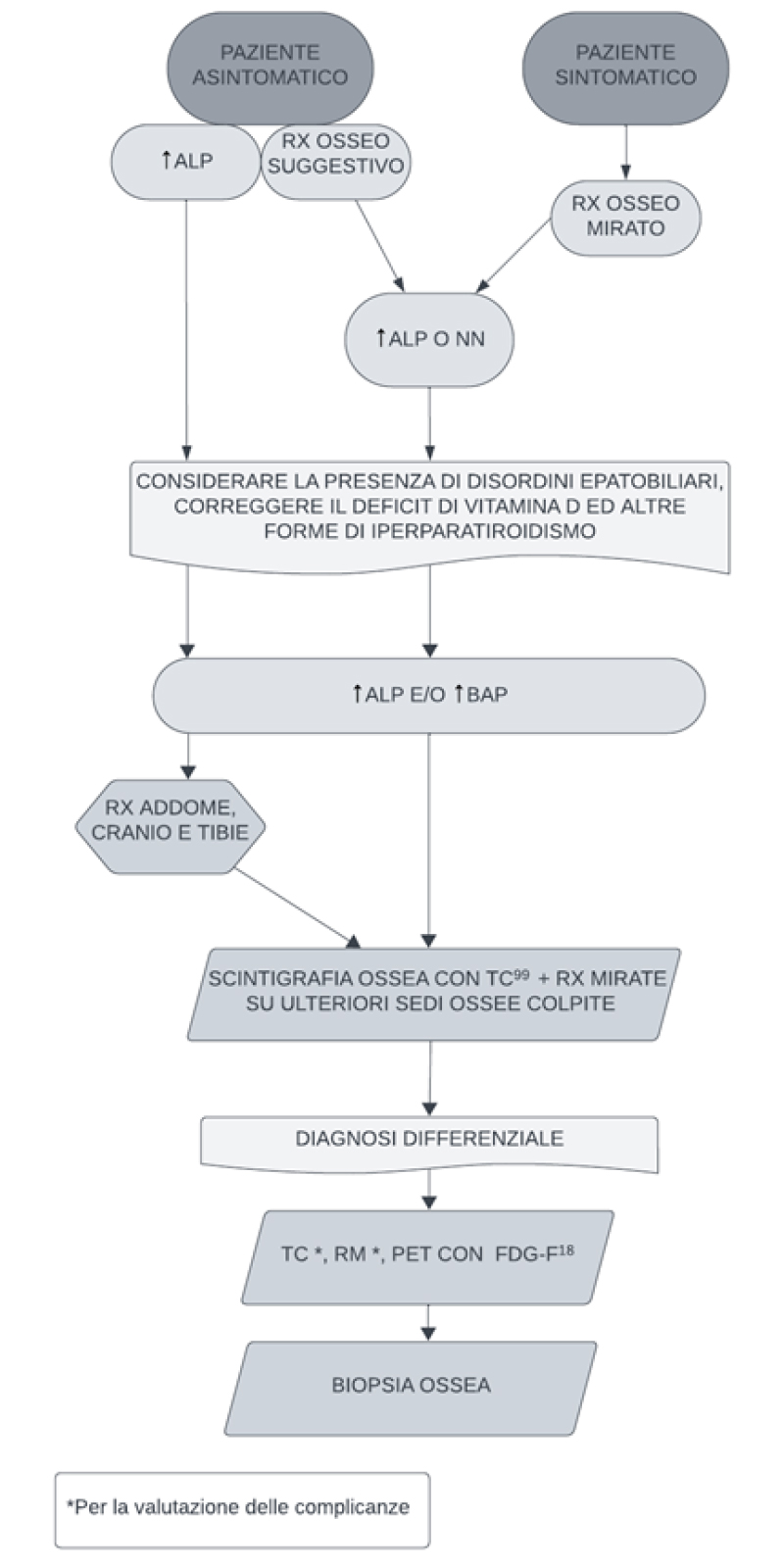 TABELLA 1. Farmaci e schemi di terapia raccomandati nella Malattia di Paget
TABELLA 1. Farmaci e schemi di terapia raccomandati nella Malattia di Paget
Conflitto di interesse Gli autori dichiarano di non avere conflitti di interesse.
Consenso informato Lo studio presentato in questo articolo non ha richiesto sperimentazione umana.
Studi sugli animali Gli autori di questo articolo non hanno eseguito studi sugli animali
Riferimenti bibliografici
- Gennari L, Di Stefano M, Merlotti D et al (2005) Prevalence of Paget’s disease of bone in Italy. J Bone Miner Res 20: 1845-1850
- Ralston SH, Corral-Gudino L, Cooper C et al (2019) Diagnosis and management of Paget’s disease of bone in adults: a clinical guideline. J Bone Miner Res 34: 579-604
- Singer FR, Bone HG, Hosking DJ et al (2014) Paget’s disease of bone: an endocrine society clinical practice guideline. J Clin Endocrinol Metab 99: 4408-4422
- Barale M, Cappiello V, Ghigo E et al (2019) Increased frequency of impaired fasting glucose and isolated systolic hypertension in Paget’s disease of bone. Endocrine 63:385–390
- Barale M, Sigrist S, Bioletto F et al (2021) Long-term efficacy of intensive zoledronate therapy and predictors of retreatment in Paget’s disease of bone. Calcified Tissue Int 109:383–392
Scarica Articolo PDF



