Il monitoraggio continuo del glucosio a scansione intermittente (FGM) nel diabete tipo 2
Annalisa Giandalia, Alessandro Cuttone
Dipartimento di Medicina Clinica e Sperimentale, Università degli Studi di Messina, Messina, Italia Autore corrispondente A.Giandalia agiandalia@yahoo.it
Abbreviazioni: DM2, diabete mellito di tipo 2; rtCGM, real-time Continuous Glucose Monitoring; SMBG, self-monitoring of blood glucose; FGM, Flash Glucose Monitoring; TIR, Time in range.
Introduzione
L’automonitoraggio della glicemia è considerato un vero e proprio strumento terapeutico, utile ad ottimizzare il controllo glicemico nei soggetti affetti da diabete mellito, perché consente la verifica periodica del raggiungimento dei target glicemici e quindi l’adeguamento della terapia (farmacologica o nutrizionale).
Nell’ultimo decennio sono stati sviluppati dispositivi tecnologici in grado di monitorare in continuo i livelli di glucosio nel liquido interstiziale, attraverso un sensore sottocutaneo, fornendo una lettura della glicemia in “real time” (rtCGM, real-time Continuous Glucose Monitoring) oppure in modo intermittente “on-demand” grazie all’ausilio di specifici scanner (FGM, Flash Glucose Monitoring). Il loro impiego è diffuso e consolidato nel diabete di tipo 1 ma, negli ultimi anni, le evidenze scientifiche disponibili e l’esperienza clinica ormai vasta, hanno portato ad un’espansione del loro utilizzo anche nei soggetti con diabete di tipo 2 (DM2), soprattutto se in trattamento insulinico o con ipoglicemie severe o inavvertite.
Non stupisce, quindi, che anche i recenti Standard di Cura dell’American Diabetes Association (ADA) ne raccomandino l’uso nel DM2 in trattamento insulinico [1].
Per quanto riguarda, in particolare, il sistema FGM, che è quello più ampiamente utilizzato nel DM2 anche per ragioni di costi, diversi studi clinici randomizzati e Real World ne hanno valutato l’efficacia e la sicurezza nei soggetti affetti da DM2, in confronto al monitoraggio tradizionale (SMBG, self-monitoring of blood glucose). Tali evidenze dimostrano benefici sui livelli di HbA1c e sul rischio di ipoglicemia, con riduzione del tempo trascorso in ipoglicemia e del numero di eventi ipoglicemici diurni e notturni, in popolazioni eterogenee di pazienti, in trattamento con insulina o ipoglicemizzanti orali [2-4].
Benefici clinici
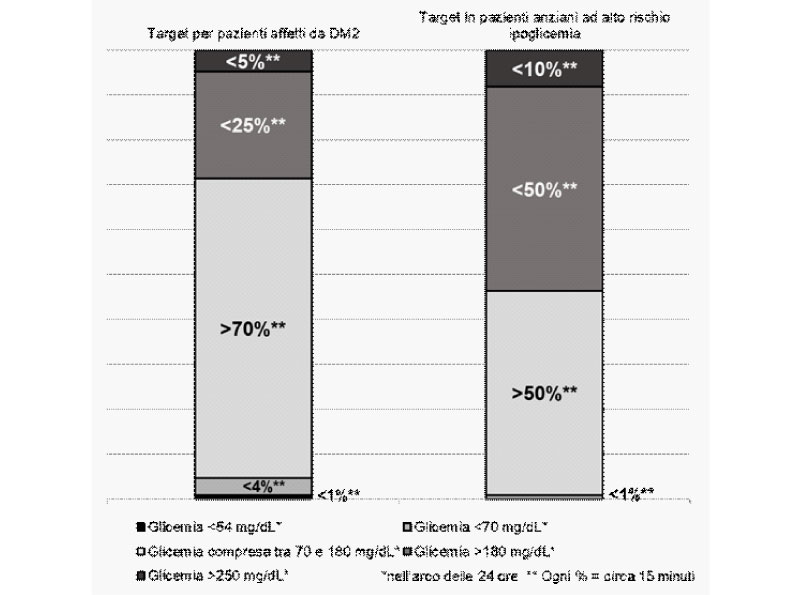
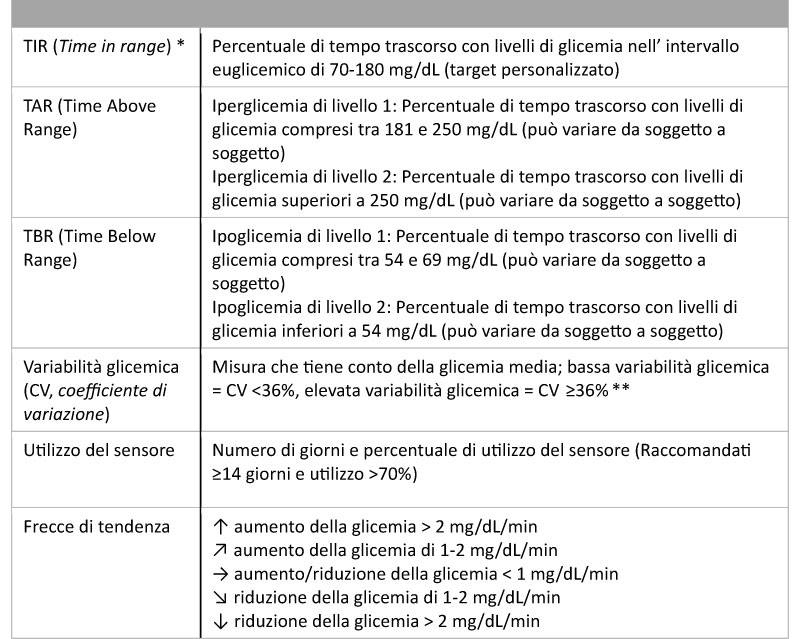
L’utilizzo della tecnologia FGM permette la valutazione di parametri complementari alle informazioni derivanti dal SMBG e dal dosaggio della HbA1c, per i quali esistono oggi metriche standardizzate e obiettivi raccomandati [1,5]; tra questi, il Time In Range (TIR) ovvero il tempo trascorso dal paziente con valori compresi nell’intervallo glicemico predefinito, la frequenza degli episodi di ipoglicemia o iperglicemia e la variabilità glicemica, che riflette l’ampiezza e la frequenza delle escursioni glicemiche (tabella 1 e figura 1).
Diverse evidenze suggeriscono che l’elevata variabilità glicemica si associ a peggiori outcomes clinici e incremento del rischio di eventi cardiovascolari nel DM2 [6] e che il solo dosaggio dell’Hba1c presenti dei limiti e fornisca informazioni non sempre sufficienti (tabella 2).
Il monitoraggio FGM consente ai medici che hanno in cura il paziente, di individuare le fluttuazioni della glicemia, conoscere i momenti della giornata in cui si verificano, identificare criticità nella gestione del diabete e personalizzare la terapia; permette, inoltre, di educare il paziente stesso a gestire le escursioni glicemiche adattando la terapia ai cambiamenti dello stile di vita e alle necessità legate, per esempio, allo sport e all’alimentazione.
Un elemento di grande utilità pratica è la presenza di “frecce di tendenza”, che esprimono la direzione della glicemia al momento della rilevazione e consentono di prevedere l’entità della variazione glicemica al minuto (tabella 1). La presenza di allarmi e avvisi (disattivabili) al raggiungimento di soglie preimpostate e modificabili permette, inoltre, di ridurre il rischio di ipoglicemia e iperglicemia imprevista e ridurre la variabilità glicemica.
Tutto questo si traduce in un miglioramento dell’aderenza terapeutica, della qualità della vita del paziente e del grado di soddisfazione verso la terapia misurata tramite questionario DTSQ (Diabetes Treatment Satisfaction Questionnaire) [4], parametri che influenzano in modo significativo il raggiungimento degli obiettivi terapeutici.
Gli eventi avversi più comuni sono le reazioni cutanee sul sito di applicazione, prurito, allergia, eruzione cutanea. Altri potenziali limiti sono il rischio di correzione eccessiva dei valori glicemici anormali da parte dei pazienti e il possibile impatto negativo degli allarmi sul benessere psicologico (stress e affaticamento da allarmi). D’altro canto, il corretto utilizzo dei dispositivi per il FGM richiede un processo iniziale e continuo di educazione e formazione del paziente, da parte dell’equipe specialistica, sulle operazioni connesse con la misurazione della glicemia, l’interpretazione dei dati e l’autogestione della terapia.
Conclusioni
In conclusione, la tecnologia FGM, grazie anche alla sua accuratezza e facilità di impiego, può rappresentare uno strumento clinico utile nella gestione dei soggetti con DM2 in trattamento insulinico, permettendo di migliorare il compenso glicemico, la compliance e la consapevolezza del paziente, di ridurre il rischio di ipoglicemia e di migliorare la sua qualità della vita.
Figura 1. Obiettivi glicemici nei soggetti in monitoraggio continuo del glucosio
Modificata da Battelino T et al. [5] NB Obiettivi meno ambiziosi sono raccomandati nei pazienti anziani e/o fragili e nei soggetti ad alto rischio di ipoglicemia a causa dell’età, della durata del diabete e della terapia.
Tabella 1. Metriche del monitoraggio glicemico in continuo
Modificata da Battelino T et al. [5]
*Per poter determinare il TIR è opportuno utilizzare i dati glicemici rilevati per almeno 14 giorni.
Ad un aumento del 10% del TIR corrisponde una riduzione dello 0,8% dei livelli di HbA1c
** bassa variabilità glicemica = CV <33% secondo alcuni Autori
Tabella 2. Limiti dell’HbA1c
Conflitti di interesse Gli autori dichiarano di non avere conflitti di interesse
Consenso informato Lo studio presentato in questo articolo non ha richiesto sperimentazione umana.
Studi sugli animali Gli autori di questo articolo non hanno eseguito studi sugli animali
Riferimenti bibliografici
- American Diabetes Association. Diabetes Technology: Standards of Care in Diabetes—2023. Diabetes Care December 2022, Vol.46, S111-S127. doi:https://doi.org/10.2337/dc23-S007
- Haak T, Hanaire H, Ajjan R, Hermanns N, Riveline JP, Rayman G. Flash Glucose-Sensing Technology as a Replacement for Blood Glucose Monitoring for the Management of Insulin-Treated Type 2 Diabetes: a Multicenter, Open-Label Randomized Controlled Trial. Diabetes Ther 8:55–73, 2017.
- Krakauer M, Botero JF, Lavalle-González FJ, Proietti A, Barbieri DE. A review of flash glucose monitoring in type 2 diabetes. Diabetol Metab Syndr. 2021 Apr 9;13(1):42. doi: 10.1186/s13098-021-00654-3. PMID: 33836819; PMCID: PMC8035716.
- Yaron M, Roitman E, Aharon-Hananel G, Landau Z, Ganz T, Yanuv I, Rozenberg A, Karp M, Ish-Shalom M, Singer J, Wainstein J, Raz I.Effect of Flash Glucose Monitoring Technology on Glycemic Control and Treatment Satisfaction in Patients With Type 2 Diabetes. Diabetes Care 1 July 2019; 42 (7): 1178–1184.
- Battelino T, Danne T, Bergenstal RM et al. Clinical Targets for Continous Glucose Monitoring Data Interpretation: Recommendations From The International Consensus on Time in Range. Diabetes Care 42:1593-1603, 2019
- Ceriello A, Monnier L, Owens D. Glycaemic variability in diabetes: clinical and therapeutic implications. Lancet Diabetes Endocrinol. 2019 Mar;7(3):221-230. doi: 10.1016/S2213- 8587(18)30136-0. Epub 2018 Aug 13. PMID: 30115599. 37(15_suppl):e17578–e17578.
Scarica Articolo PDF